�z��n-�������e-
�����Љ�i�S���ǃC���^�[�x���V�����O���[�v�j
1. ����
�������C���^�[�x���V�����Ɋ֘A���āA�S���ǃC���[�W���O�y�S��CT�EMRI,���Ǔ������g(IVUS),�����f�w�@(OCT)�z��v���b�V���[���C���[�E�h�b�v���[�t���[���C���[��p���������I�������d�Ǔx�]����ϋɓI�ɍs���A����������ɑ��Č`�ԓI�A�g�D�w�I�A�@�\�I�ȃA�v���[�`�����Ă���B�����̉�͂���l�X�ȗՏ��������s���Ă���A���ɐS�t�A�ւƂ��Ė����t���a�ⓧ�͏Ǘ�ɂ����銥�����C���^�[�x���V�������ÂɊւ��錤���ł͉Ȍ�����l�����Ă���B�܂��A�����������̃��X�N�t�@�N�^�[�ł��郁�^�{���b�N�nj�Q�̕a�ԁE���ÂɊւ��Ă̌������s���Ă���B�������ʂ͍��������łȂ��C�O�̎�v�w���p���W���[�i�����ɂ����Ė��N���\���s���Ă���B���{���������ɂ��ϋɓI�ɎQ�����Ă���A���@�̎��̍����f�[�^�����������łȂ��C�O�ɂ����M���A���ʂ������Ă���B
�������Ǘ̈�̎��Âł́A���ɐt���ǐ��������ɑ��ē��@�t���O���[�v�Ƌ��͂��Đf�f���Â��s���A���̕a�Ԃ⎡�ÂɊւ��Ă̗Տ��������s���Ă���B
2. ���@��
1) ��w������
3-4�N���̌n���u�`�ɂ����āA�S���J�e�[�e���@�A�S�V���`�@�Ȃǂ̉摜�f�f�A�������ǂƍ������ǂ̊��댯���q�A�������S���a�̊e�_�Ȃǂ�S�����Ă���B
2) ���㋳��
����Տ����C�i���C����j�ł́A�S���J�e�[�e���@�̊�b�I�Ȑf�f��Z���͕��@���w�ԁB���ɁA�ҋ@�I�ȐS���J�e�[�e���ɂ����ẮA�p�҂Ƃ��đ�����̌o����ςނ��Ƃ�ڕW�ɂ��Ă���B�܂��A�ً}�J�e�ɂ�����f�f��Z���o�������p�҂Ƃ��ĎQ��������悤�ɔz�����Ă���B���nj`���p�ɂ��āA����Ƃ��Ċԋ߂Ȍo����ςނ��Ƃ��o����B���ɁA�}���̎�舵���ɂ��ẮA�����A��������w����ƂƂ��ɏ����f�f�A���Â��o�����A�ً}�S���J�e�[�e���@�ւ̈�A�̉ߒ��ɏK�n�ł���悤�ɔz�����Ă���B�܂����nj`���p�Ɋւ��ẮA�V�~�����[�^�[��p���������N1-2��A�Ǘጟ������w����Z�b�V�������J�Â��A�ϋɓI�ɎQ�����Ă��炤�悤�ɂ��Ă���B
3) ��w�@����
��]�҂͑�w�@�ɓ��w���A�Տ��f�[�^�̌����E��͂�i�߂Ę_�����쐬���Ċw�ʂ��擾���Ă���B�܂���b��w�����Ƃ̘A�g������ł���A���̈�̊�b�������s�����Ƃ��\�ł���B
�����Љ�i�S�s�S�E�S�G�R�[�O���[�v�j
1. �Տ�����
�R�����o���ǂ���ьo�H���S�G�R�[�}������p���A�S�@�\�E�ٖ��ǁE�o���ǃG�R�[�ɂ�銥���������]�����A���L������ł̗Տ��������s���Ă���B���ɁA�m�X�ًt���E�m�X�و�E�ǁA��ِ��ᗬ�ʒሳ�r���d�Ǒ哮���ً���ǂɊւ��錤���ł́A�Ȍ�����l�����A�����O�̊w�p�W��ւ̔��\�A�_���f�ڂ��s���Ă���B�������m�X�ًt���̊�{�@�����u�����g��ɂ��������O���֕ψʂ��A���̓������ِ���ُ�ɋ�����������(tethering)�v�ł��邱�Ƃ̉𖾂́A���̌�̋@�\���m�X�ًt���̕a�Ԑ����̉𖾁A����і��Â̊J���ɖ𗧂Ă��Ă���B
2. ���@��
1) ���O����
�w���u�`�ɐS�G�R�[�̃f�W�^�������p���Č��ʂ̂��鋳������H���Ă���B�|���N���ł́A�S�G�R�[�̑����̓�����g���A���^������ʂ��Č����悭���炵�Ă���B�܂��A�G�R�[���K���s���A�w�����S�G�R�[���������[�������ł���悤�ɂ��Ă���B
2) ���㋳��
�Տ��J���t�@�����X�ł́A���ƂȂ�Ǘ�̐S�G�R�[�}�������������A�摜���߂�Ǘ�̕a�ԂɊւ��Đ[���c�_���s���Ă���B�S�G�R�[�J���t�@�����X���s���A�摜���ߓ��Ŗ��ƂȂ����Ǘ��������������[�߂Ă���B���C����́A�o���ǐS�G�R�[�E���ǃG�R�[�E�o�H���S�G�R�[�E���אS�G�R�[�Ɍg���A�m���E�Տ��o���Ƃ��Ɍ��r���d�˂Ă���B
3) ��w�@����
��]�҂́A��w�@�ɓ��w���A�Տ������̒������́E������i�߂āA�_�����쐬���A�w�ʂ��擾���Ă���B
�����Љ�i�s�����O���[�v�j
�Տ������E��b�����݂̂Ȃ炸�Y�ƈ�w�I�������s�Ȃ��Ă��܂��B�����̌����́A�����J���Ȋw������⏕���E�J�����S�q�������������Ƃ╶���Ȋw�ȉȊw������⏕���E��Ռ����ɂ���đ����̌�������l�����Ă��܂��B
1. �Տ���w�I����
1) �y�[�V���O���ʂƌ��s���ԂɊւ��錤��
�y�[�V���O���ÂɊւ����K�͗Տ������ɂ��A�]������Ȃ���Ă����E���S�땔�y�[�V���O���A������dessynchrony�������炵�A�S�s�S�����������Ƃ����炩�ƂȂ��Ă��܂����B���Ȃł�2003�N���E���S�땔���璆�u�y�[�V���O�ɕύX���A���s���Ԃɋy�ڂ��L�v�����ό��I����ɂ�茟�����Ă��܂��B�����̌������ʂ́A�č�Heart Rhythm Society�ACardiostim�ACardiRhythm����{�s�����w��A���{�z��w��Ő��������Ă���݂̂Ȃ炸�A���ۊw�p���ɂ������������ʂ��f�ڂ���Ă��܂��B�i�����J���Ȋw�����j
2) �y�[�X���[�J�nj�Q�̔��Nj@��
�y�[�V���O���ʂƗ��߂Ĕ��I�y�[�V���O���[�h�Ŕ�������y�[�X���[�J�nj�Q�̋@�����������Ă��܂��B�i�����J���Ȋw�����j
3) ���njS�[�ד��̌���
�y�[�X���[�J�������[�@�\��p���Ė��njS�[�ד��̔����p�x��v���ɂ��Ă̌������s�Ȃ��Ă��܂��B
4) �_�o���ߐ����_���҂̃g���[�j���O����
�_�o���ߐ����_�͎��_�̌��������Ƃ��čł��������A���Ȃł͔���ÂƂ��Ċ��҂��܂������E��ɂ����Ď����ōs�Ȃ����Ƃ��o����g���[�j���O���Ö@���J�����A�������Ì��ʂĂ���B�_�o���ߐ����_�̃g���[�j���O���Â͍����ł͓��Ȃ��ł��i��ł���B�{�g���[�j���O���Â̌��ʂɂ��Ă͍����O�̈ꗬ���ɐ������̌������ʂ���Ă��܂��B�i�����Ȋw�Ȋ�Ռ����A�����J���Ȋw�����j
5) �d�NjN�����ጌ�����҂ɑ���y�[�V���O����
�d�NjN�����ጌ�����҂ɂ͋ɂ߂ėL���Ȏ��Ö@���Ȃ��̂�����ł��B���Ȃł́A�����̊��҂Ƀy�[�V���O���Â������Ȃ����ƂŁA�Ǐ�̉��P���ʂ������邱�Ƃ���O�̊w��݂̂Ȃ炸�ꗬ���ې�厏�ɂ����Ă��܂��B�i�����J���Ȋw�����j
6) ICD���҂̏A�J�Ɋւ��钲������
�����ɂ�����ICD���҂̏A�J�Ɋւ�����Ԓ�������{�s�����S�d�w��̃f�o�C�X�ψ���ƍ����ōs�Ȃ��Ă��܂��B�i�����J���Ȋw�����j
7) ���̓��f�o�C�X���҂Ɠd������
���̓��A���݃f�o�C�X�ɋy�ڂ��d��������ː�CT�̋y�ڂ��e���ɂ��Ď����I�Ɍ������s�Ȃ��Ă��܂��B�i�����J���Ȋw�����j
8) ���_���҂̗\��ƏA�J
���_���҂̗\��ƏA�J�Ɋւ��钲�������𑽎{���������ōs�Ȃ��Ă��܂��B�i�����J���Ȋw�����A�����Ȋw�ȉȌ�����j
9) �f�o�C�X���҂̏A�J�Ɨ����x��
�f�o�C�X�A���݊��҂Ȃǂ��܂ޏz�펾�����҂ɑ��鎡�ÂƏA�J�̗����Ɋւ��錤�����s���Ă��܂��i�����J���Ȋw�����j�B���̐��ʂɂ��u�S�����̎��ÂƎd���̗������𗧂��m�[�g�v�̊��s������J���Ȃ��甭�s����Ă��闼���x���A�g�}�j���A���ɔ��f����Ă��܂��B
10) ��x�Ö��������S�[�ד��ɂ�������Ö��̊�^�Ɋւ��錤��
�S�[�ד��J�e�[�e���A�u���[�V�������{�s���銳�҂�Ώۂɏ��Ö��̓d�C�����w�I�����Ƃ��̕s���������Ɋւ���@�����𖾂��錤�����s���Ă��܂��B
11) �J�e�[�e���A�u���[�V�������ɔ��������C�ǐ��̋@����
���{�s�����S�d�w���蒍�ӊ��N�����o���ꂽ�J�e�[�e���A�u���[�V�������̋�C�ǐ��Ɋւ��Ď����I�������s�����̋@�����𖾁AJournal of Cardiovascular Electrophysiology�ɔ��\���Ă��܂��B
12) �A�J����ɂ�����@�O�S�x��~�̓����Ɋւ��錤��
�{�M�ɂ�����A�J����̕��ϔN��̏㏸�A��N�����܂��āA���h���f�[�^����͂������ɓn��A�J����̉@�O�S�x��~�̓�����X���Ɋւ��錤�����s���Ă��܂��B
2. ��b��w�I����
1) �S���ˑR���̌����ƂȂ�v�����s�����̔��ǃ��J�j�Y���ɂ��āA�S�؍זE���x���ł̌������s�Ȃ��Ă��܂��BQT�����nj�Q��Brugada�nj�Q�Ȃǂ̈�`�w�I�f�������s�����ɂ��āA�d�C�����w�I��@��p���ăC�I���`���l���̋@�\��͂��s�Ȃ��A�Տ����Ɍ��т����ݓI�������@�����������Ă��܂��B�܂��A��ܐ�QT�����nj�Q�̋@���𖾂��������x���ōs�Ȃ��Ă��܂��i�����Ȋw�Ȍ����j�B �܂��A������V�[�P���T�[��p���Ĉ�`�I�s���������̈�`�q��͂ƕa�ԉ𖾂Ɋւ��錤�����s���Ă��܂��B
3. ����
1) ��w������
��w������͂R�`�S�N���ɂ�����z��u�`�̂Ȃ��ŁA�S�d�}�A���אS�d�}�A�������S�����̐S�d�}�f�f�A�������s�����A�p�����s�����̂T�R�}��S�����Ă��܂��B�U�N�����ɂ͑����u�`�Ƃ��āu�S���ˑR���Ǝ��_����v��S�����Ă��܂��B
2) ���㋳��
����Տ��C����ɑ��āA�z�펾�����ɕs���������Ɋւ��ẮA�@���Ŏ{�s���ꂽ�S�d�}�A�z���^�[�S�d�}�A�^�����אS�d�}�̔��ǂ�ʂ��ė�����[�߁A���m�ȐS�d�}���ǂ��o����悤�Ɏw�����Ă��܂��B�܂��A�y�[�X���[�J�A���ݎ�p��v���O���}�[�̊Ǘ��E����A�J�e�[�e���S�؏Ďp�ɂ�����S���S�d�}�̔��ǂ�AICD��CRT-D�̎�Z�E�Ǘ�����ϋɓI�ɍs�Ȃ��A���̒��g�������ł���l���炵�Ă��܂��B���_���҂�head-up tilt�������S�������A���_�̐f�f�E���Â���l�ōs�Ȃ���悤�Ɏw�����Ă��܂��B�܂��A��������Ǘ��Տ������̈ꕔ�͐ϋɓI�Ɋw��\���s�Ȃ킹�A�w�p�_���쐬���w�����Ă܂��B�Տ���������́APACE���AJ Cardiovasc Electrophysiol���ACirculation J���AJ Cardiovasc Pharmacol�����ɑ����̘_�����f�ڂ��A�����̌����ɂ�葽���̏C���オ�w�ʎ擾���s�Ȃ��Ă��܂��B�܂��A���ȏȉȌ����������J���Ȋw�����ɂ��ϋɓI�ɎQ�������A�Ő�[�Տ������݂̂Ȃ炸�Y�ƈ�w�I�����ɂ��Q�������Ă��܂��B���C����I�����_�ł̏z�����Ɗw�ʎ擾�A����ɓ��{�s�����S�d�w��̕s��������擾��ڎw���Ďw�����Ă��܂��B
3) ��w�@����
�s�����O���[�v�ɏ������A��w�@����]�����t�ɂ́A�O�q�̗l�ɓd�C�����w�̊�b�y�їՏ��I�m���A���ÁE�f�o�C�X��p��J�e�[�e���A�u���[�V�����ȂǕs��������Ƃ��Ă̒m���E�f�ËZ�p�̏K���ƂƂ��ɁA�Տ����瓾��ꂽ�A�C�f�B�A����������Տ������E�������s���A����܂ňꗬ���ɐ������̌������ʂ���Ă��܂��B
�����Ɛ�
�ŐV�̋Ɛт͈�Ǖւ�������������B
��Ǖւ�͂�����B
PDF�ɂċL�ڂ��Ă���܂��B
- (1997�N�`2008�N)�������E�����d���O���[�v.pdf
- (1997�N�`2008�N)�S�s�S�E�S�G�R�[�O���[�v.pdf
- (1997�N�`2008�N)�s�����O���[�v.pdf
��PDF�������ɂȂ�ɂ�Adobe Reader���K�v�ł��B
�����Љ�i��b�����j
�͂��߂�

�@�Y�ƈ�ȑ�w��2���Ȋw�A��b�������͕Љ��됰�����̃T�|�[�g�̉��A2022�N4���ɃX�^�[�g���܂����B��������C�̌É��Harvard��w�ABrigham and Women�fs�a�@�ɗ��w������A��B��w�z����Ȃɂ����ĐS���Ǖa�̕a�Ԃɂ�����}�N���t�@�[�W�������@�\�𒆐S�Ɋ�b�������s���ĎQ��܂����B
�@���C��A2�������o�߂����������ł����̐搶���𒆐S�Ɏ������J�n���܂����B���������ł͂���܂ōs���Ă����}�N���t�@�[�W�������@�\�Ɋւ����b�����ɉ����A��b�����̐��ʂ�Տ����p���邽�߂̃g�����X���[�V���i�����T�[�`�ȂǗՏ��̋��������炱���s���錤����W�J�������Ǝv���Ă��܂��B
�@�����K���a�ɋN������z�펾���A�t�����̌����ɂ������̂�����������܂������2���Ȉ�ǂ܂ł��A���������B��w�@�ւ̐i�w���l���Ă�����搶�����}�������܂��B
2022�N5��18��
�Y�ƈ�ȑ�w��2���Ȋw
�w���u�t�@�� ����Y
�������e
�S���Ǖa�̔��ǁE�i�W���J�j�Y���ɂ�����~�g�R���h���A�_�C�i�~�N�X�̖�����
�@�~�g�R���h���A�͍זE���G�l���M�[��ӂɂ����Ē��S�I������S���זE�����튯�ł����A���̓��ɂ����ĕ����Z�����J��Ԃ����X�Ƃ��̌`�Ԃ�ω������Ă��邱�Ɓi�~�g�R���h���A�_�C�i�~�N�X�j���m���Ă��܂��B�������̓~�g�R���h���A�_�C�i�~�N�X�𐧌䂷�镪�q�̂ЂƂ�Drp1(dynamin-related protein 1)�ɒ��ڂ������d����S�؍[�ǂȂǗl�X�ȐS���Ǖa�̕a�Ԃ̒��Ń~�g�R���h���A�_�C�i�~�N�X�̉ʂ��������𖾂炩�ɂ��邱�Ƃ����݂Ă��܂�(ATVB 2020)�B
�����d���ɂ�����}�N���t�@�[�W�������@�\�̉�
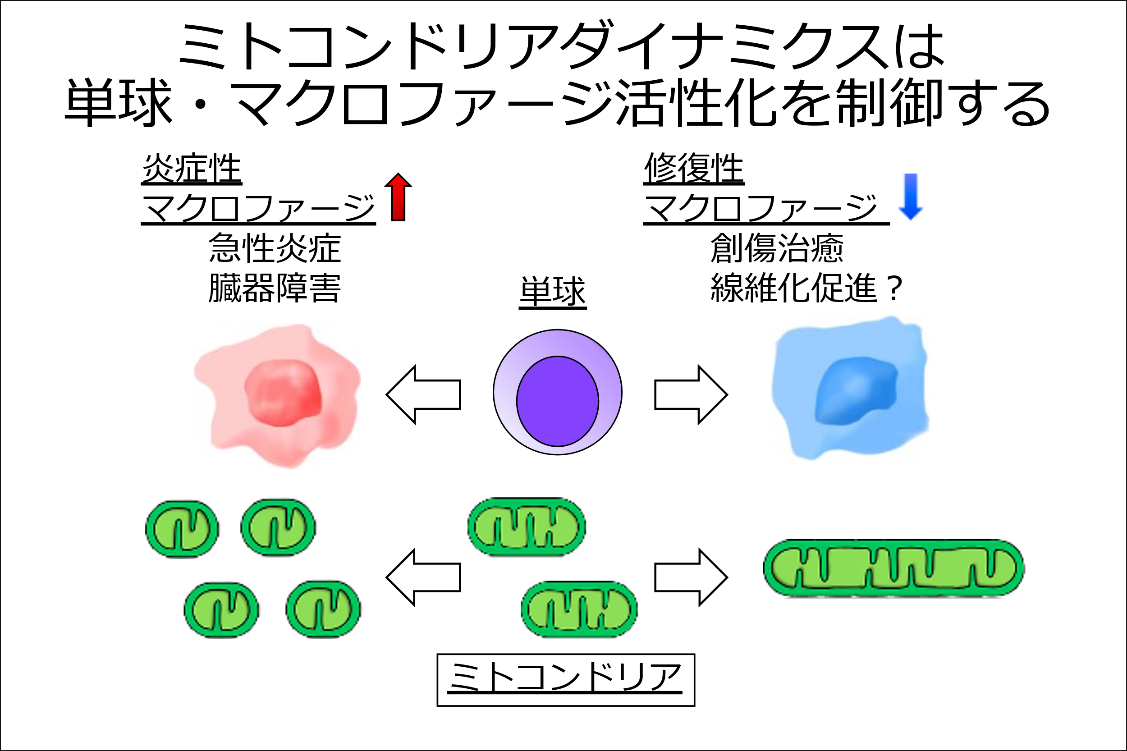
�@�}�N���t�@�[�W����鉊�ǂ͏����a�ς̌`������S�؍[�ǂȂǂ̋}�����𐫍����ǂ̔��ǂɎ���܂œ����d���̔��ǁE�i�W�v���Z�X�̒��Œ��S�I�Ȗ������ʂ����Ă��܂��B�������͂���܂ŃA���W�I�e���V���U�⌌�Ǔ��琬�����q�ȂǗl�X�ȕ��q�ɂ��}�N���t�@�[�W�������@�\�A�����d���i�W�@�\�𖾂炩�ɂ��Ă��܂���(ATVB 2008, ATVB 2015, JAHA 2016)�B
�h���b�O�f���o���[�V�X�e����p��������S���Ǖa�ɑ���V�K���ÊJ��
�@�����d���ɋN������e�펾���i�S�؍[�ǁA�]�[�ǁA�������������j�A�S�؍[�nj�̐S�s�S�Ȃnj��s�̎��Â��s���Ă����Ì��ʂ��s�\���Ȏ�����ΏۂɁA��b�����ɂ�蓾��ꂽ�m���Ɋ�Â��h���b�O�f���o���[�V�X�e����p�����V�K���Â̊J�����s���Ă��܂�(Circulation 2014, Sci Rep 2020, J Atheroscler Thromb. 2022)�B
�����o�[
�w���u�t
�� ����Y
�C���w����
��� �[��
��w�@��
�p�X ���
���� �q��
�ߓ� �S��(�S�����NJO�Ȋw�u�����)
�����⏕��
���c �q�q

�� ����Y
Jun-ichiro Koga, M.D., Ph.D.
�o��
����14�N�@��B��w��w����w�ȑ���
����14�N�@��B��w��w�������a�@�z����ȁ@���C��
����16�N�@��B��w��w�@��w�����@
����20�N�@���R�ԏ\���a�@�@�z���
����23�N�@Brigham and Women�fs�a�@�A�n�[�o�[�h��w��w���@���m������
����26�N�@��B��w��w�@��w�����@�@�z����ȁ@�w�p������
����27�N�@��B��w�z��a����������Z���^�[�@���C����
����31�N�@��B��w�a�@�@�z����ȁ@���C����
�ߘa 4�N�@ �Y�ƈ�ȑ�w��w����2���Ȋw�@�w���u�t
�����w��
���{���Ȋw��i�F���A�������Ȑ���A�w����j
���{�z��w��i����j
���{�S���ǃC���^�[�x���V�������Êw��
���{���ǐ�����w��i�]�c���j
���{�����d���w��i����A�w����A�]�c���j
���ېS��������iISHR�j���{����i�]�c���j
���{DDS�w��
American Heart Association
North American Vascular Biology Organization
�Ɛ�
�����_��
- Ikeda G, Matoba T, Ishikita A, Nagaoka K, Nakano K, Koga J, Tsutsui H, Egashira K. Nanoparticle-Mediated Simultaneous Targeting of Mitochondrial Injury and Inflammation Attenuates Myocardial Ischemia-Reperfusion Injury. J Am Heart Assoc. 2021 Jun 15;10(12):e019521.
- Katsuki S, Koga J*, Matoba T, Umezu R, Nakashiro S, Nakano K, Tsutsui H, Egashira K. Nanoparticle-Mediated Delivery of Pitavastatin to Monocytes/Macrophages Inhibits Angiotensin II-Induced Abdominal Aortic Aneurysm Formation in Apoe-/- Mice. J Atheroscler Thromb. 2022 Jan 1;29(1):111-125.
- Matsumoto T, Yoshino S, Furuyama T, Morisaki K, Nakano K, Koga J, Maehara Y, Komori K, Mori M, Egashira K. Pitavastatin-Incorporated Nanoparticles for Chronic Limb Threatening Ischemia: A Phase I/IIa Clinical Trial. J Atheroscler Thromb. 2022 May 1;29(5):731-746.
- Okahara A, Koga J*, Matoba T, Fujiwara M, Tokutome M, Ikeda G, Nakano K, Tachibana M, Ago T, Kitazono T, Tsutsui H, Egashira K. Simultaneous targeting of mitochondria and monocytes enhances neuroprotection against ischemia-reperfusion injury. Sci Rep. 2020 Sep 2;10(1):14435.
- Umezu R, Koga J*, Matoba T, Katsuki S, Wang L, Hasuzawa N, Nomura M, Tsutsui H, Egashira K. Macrophage Dynamin-Related Protein 1 Accelerates Intimal Thickening After Vascular Injury. Arterioscler Thromb Vasc Biol. 2020 Jul;40(7):e214-e226.
- Fujiwara M, Matoba T, Koga J, Okahara A, Funamoto D, Nakano K, Tsutsui H, Egashira K. Nanoparticle incorporating Toll-like receptor 4 inhibitor attenuates myocardial ischaemia-reperfusion injury by inhibiting monocyte-mediated inflammation in mice. Cardiovasc Res. 2019 Jun 1;115(7):1244-1255.
- Tokutome M, Matoba T, Nakano Y, Okahara A, Fujiwara M, Koga J, Nakano K, Tsutsui H, Egashira K. PPAR��-targeting Nanomedicine Promotes Cardiac Healing After Acute Myocardial Infarction by Skewing Monocyte/Macrophage Polarization in Preclinical Animal Models. Cardiovasc Res. 2019 Feb 1;115(2):419-431.
- Honda K, Matoba T, Antoku Y, Koga J, Ichi I, Nakano K, Tsutsui H, Egashira K. Lipid-Lowering Therapy With Ezetimibe Decreases Spontaneous Atherothrombotic Occlusions in a Rabbit Model of Plaque Erosion: A Role of Serum Oxysterols. Arterioscler Thromb Vasc Biol. 2018; 38(4): 757-771.
- Ichimura K, Matoba T, Koga J, Nakano K, Funamoto D, Tsutsui H, Egashira K. Nanoparticle-Mediated Targeting of Pitavastatin to Small Pulmonary Arteries and Leukocytes by Intravenous Administration Attenuates the Progression of Monocrotaline-Induced Established Pulmonary Arterial Hypertension in Rats. Int Heart J. 2018 Nov 28;59(6):1432-1444.
- Nakano K, Matoba T, Koga J, Kashihara Y, Fukae M, Ieiri I, Shiramoto M, Irie S, Kishimoto J, Todaka K, Egashira K. Safety, Tolerability, and Pharmacokinetics of NK-104-NP. A Multicenter, Randomized, Placebo-Controlled Phase I Investigator-Initiated Trial for Intravenous Administration of Pitavastatin-Loaded PLGA Nanoparticles (NK-104-NP) in Healthy Japanese Male Subjects. Int Heart J. 2018;59(5):1015-1025.
- Mao Y, Koga J*, Tokutome M, Matoba T, Ikeda G, Nakano K, Egashira K. Nanoparticle-mediated delivery of pitavastatin to monocytes/macrophages inhibits left ventricular remodeling after acute myocardial infarction by inhibiting monocyte-mediated inflammation. Int Heart J. 2017; 58(4): 615-623.
- Ishikita A, Matoba T, Ikeda G, Koga J, Mao Y, Nakano K, Takeuchi O, Sadoshima J, Egashira K. Nanoparticle-Mediated Delivery of Mitochondrial Division Inhibitor 1 to the Myocardium Protects the Heart From Ischemia-Reperfusion Injury Through Inhibition of Mitochondria Outer Membrane Permeabilization: A New Therapeutic Modality for Acute Myocardial Infarction. J Am Heart Assoc. 2016; 5: e003872.
- Nakashiro S, Matoba T, Umezu R, Koga J, Tokutome M, Katsuki S, Nakano K, Sunagawa K, Egashira K. Pioglitazone-Incorporated Nanoparticles Prevent Plaque Destabilization and Rupture by Regulating Monocyte/Macrophage Differentiation in ApoE-/- Mice. Arterioscler Thromb Vasc Biol. 2016; 36(3): 491-500.
- Ichimura K, Matoba T, Nakano K, Tokutome M, Honda K, Koga J, Egashira K. A Translational Study of a New Therapeutic Approach for Acute Myocardial Infarction: Nanoparticle-Mediated Delivery of Pitavastatin into Reperfused Myocardium Reduces Ischemia-Reperfusion Injury in a Preclinical Porcine Model. PLoS One. 2016; 11(9): e0162425.
- Nakano Y, Matoba T, Tokutome M, Funamoto D, Katsuki S, Ikeda G, Nagaoka K, Ishikita A, Nakano K, Koga J, Sunagawa K, Egashira K. Nanoparticle-Mediated Delivery of Irbesartan Induces Cardioprotection from Myocardial Ischemia-Reperfusion Injury by Antagonizing Monocyte-Mediated Inflammation. Sci Rep. 2016; 6: 29601.
- Tanaka S, Matsumoto T, Matsubara Y, Harada Y, Kyuragi R, Koga J, Egashira K, Nakashima Y, Yonemitsu Y, Maehara Y. BubR1 Insufficiency Results in Decreased Macrophage Proliferation and Attenuated Atherogenesis in Apolipoprotein E-Deficient Mice. J Am Heart Assoc. 2016; 5: e004081.
- Koga J, Nakano T, Dahlman JE, Figueiredo JL, Zhang H, Decano J, Khan OF, Niida T, Iwata H, Aster JC, Yagita H, Anderson DG, Ozaki CK, Aikawa M. Macrophage Notch ligand Delta-like 4 promotes vein graft lesion development: implications for the treatment of vein graft failure. Arterioscler Thromb Vasc Biol. 2015; 35(11): 2343-53.
- Shibasaki M, Wang JG, Figueiredo JL, New SE, Quillard T, Goettsch C, Koga J, Sonoki H, Matsumoto J, Aikawa M, Aikawa E. Pitavastatin reduces inflammation in atherosclerotic plaques in apolipoprotein E-deficient mice with late stage renal disease. PLOS ONE. 2015; 10(9): e0138047.
- Katsuki S, Matoba T, Nakashiro S, Sato K, Koga J, Nakano K, Nakano Y, Egusa S, Sunagawa K, Egashira K. Nanoparticle-mediated delivery of pitavastatin inhibits atherosclerotic plaque destabilization/rupture in mice by regulating the recruitment of inflammatory monocytes. Circulation. 2014; 25; 129(8): 896-906.
- Koga J, Matoba T, Egashira K, Kubo M, Miyagawa M, Iwata E, Sueishi K, Shibuya M, Sunagawa K. Soluble Flt-1 gene transfer ameliorates neointima formation after wire injury in flt-1 tyrosine kinase-deficient mice. Arterioscler Thromb Vasc Biol. 2009; 29(4): 458-464.
- Kubo M, Egashira K, Inoue T, Koga J, Oda S, Chen L, Nakano K, Matoba T, Kawashima Y, Hara K, Tsujimoto H, Sueishi K, Tominaga R, Sunagawa K. Therapeutic neovascularization by nanotechnology-mediated cell-selective delivery of pitavastatin into the vascular endothelium. Arterioscler Thromb Vasc Biol. 2009; 29(6): 796-801.
- Koga J, Egashira K, Matoba T, Kubo M, Ihara Y, Iwai M, Horiuchi M, Sunagawa K. Essential role of angiotensin II type 1a receptors in the host vascular wall, but not the bone marrow, in the pathogenesis of angiotensin II-induced atherosclerosis. Hypertens Res. 2008; 31(9): 1791-800.
- Ihara Y, Egashira K, Nakano K, Ohtani K, Kubo M, Koga J, Iwai M, Horiuchi M, Gang Z, Yamagishi S, Sunagawa K. Upregulation of the ligand-RAGE pathway via the angiotensin II type I receptor is essential in the pathogenesis of diabetic atherosclerosis. J Mol Cell Cardiol. 2007; 43(4): 455-64.
- Egashira K, Nakano K, Ohtani K, Funakoshi K, Zhao G, Ihara Y, Koga J, Kimura S, Tominaga R, Sunagawa K. Local delivery of anti-monocyte chemoattractant protein-1 by gene-eluting stents attenuates in-stent stenosis in rabbits and monkeys. Arterioscler Thromb Vasc Biol. 2007; 27(12): 2563-8.
Editorial
- Katsuki S, Koga J. Mitochondrial Uncoupling: A Fine-Tuning Knob for Mitochondria-Targeting Therapeutics for Coronary Artery Disease. J Atheroscler Thromb. 2021 (Online ahead of print)
�p������
- Matsumoto T, Yamashita S, Yoshino S, Kurose S, Morisaki K, Nakano K, Koga J, Furuyama T, Mori M, Egashira K. Therapeutic Arteriogenesis/Angiogenesis for Peripheral Arterial Disease by Nanoparticle-Mediated Delivery of Pitavastatin into Vascular Endothelial Cells. Ann Vasc Dis. 2020;13(1):4-12.
- Kastuki S, Matoba T, Koga J, Nakano K, Egashira K. Anti-inflammatory Nanomedicine for Cardiovascular Disease. Front Cardiovasc Med. 2017; 4: 87.
- Matoba T, Koga J, Nakano K, Egashira K, Tsutsui H. Nanoparticle-mediated drug delivery system for atherosclerotic cardiovascular disease. J Cardiol. 2017 Apr 13; 70(3); 206-211. pii: S0914-5087(17)30092-8.
- Nakano T, Fukuda D, Koga J, Aikawa M. Delta-Like Ligand 4-Notch Signaling in Macrophage Activation. Arterioscler Thromb Vasc Biol. 2016; 36(10): 2038-2047.
- Koga J, Matoba T, Egashira K. Anti-inflammatory Nanoparticle for Prevention of Atherosclerotic Vascular Diseases. J Atheroscler Thromb. 2016; 23(7): 757-765.
- Koga J, Aikawa M. Crosstalk between macrophages and smooth muscle cells in atherosclerotic vascular diseases. Vascul Pharmacol. 2012; 57: 24-28.
�a�������E����
- �I��N��, �Éꏃ��Y, �]������, ����T�V. �z�펾���ɑ���h���b�O�f���o���[�V�X�e���̉\��. ������w. 37(5): 788-794, 2019.
- �r�c�����Y, �Éꏃ��Y, �]������. �V�N���t�B�����ƐS�s�S. ���{���. 76(������9): 186-190, 2018.
- �Éꏃ��Y. �~�g�R���h���A�_�C�i�~�N�X�ƐS���Ǖa. �z�����. 27: 32-25, 2018.
- ����o, �Éꏃ��Y, �]������. �i�mDDS���Â̋��n������. CARDIAC PRACTICE. 28(3): 197-201, 2017.
- �Éꏃ��Y, �]������. ���J�j�J���X�g���X�Ɠ����d�� - �R���ǃi�m���q�ɂ�鎡�Ð헪. ��w�̂����. 2016; 257(10): 969-974.
- �I��N��, �Éꏃ��Y, ����o, �]������. �}���S�؍[�ǂɑ���i�mDDS�̊J��. �ŐV��w. 2015; 70(11): 2197-2204.
- �Éꏃ��Y, ��������. �}�N���t�@�[�W�̕��q�C���[�W���O�Ɛf�f�ւ̓W�]�@��w�̂����2013; 246: 971-976.
- �Éꏃ��Y, ��������. ��17�� IV. ������̌��lj摜��� �����d���̕��q�C���[�W���O�@The Lipid�@2013; 24: 189-192.
- �Éꏃ��Y�A��������. MRI�ɂ�铮���d���̕��q�C���[�W���O. Annual Review �z�� 2013; 106-112.
- �Éꏃ��Y�A��������. �o�C�I�}�[�J�[�ƕ��q�C���[�W���O�@Heart View 2012; 16: 300-305.
- �I��N��, �Éꏃ��Y, �]������. �A���W�I�e���V��II�ɂ�鉊�ǂƓ���@�\��Q�@��w�̂���� 2009; 228(5): 439-445.
- �I��N��, �Éꏃ��Y, �]������. �v���[�N�j�]�̃i�m����.�@���q�S���Ǖa 2009; 10: 162-166.
- �Éꏃ��Y, �]������. �z�펾���ɂ�����MCP-1�̏d�v��-�����d���������𒆐S��.�@��w�̂���� 2007; 221: 1190-1194.
- �I��N��, �Éꏃ��Y, �]������. �P���J�C���Ɠ����d��.�@��w�̂���� 2007; 223: 1205-1210.
- �Éꏃ��Y, �]������. �哮��ᎂ̕��q���J�j�Y��.�@���q�S���Ǖa 2007; 8: 16-21.
- �Éꏃ��Y, �I��N��, �]������. �哮��ᎂ̕��q���J�j�Y��.�@Angiology Frontier 2007; 6: 306-312.
�w��\
- Koga J, Katsuki S, Matoba T, Tsutsui H. Mitochondrial dynamics in macrophage-mediated inflammation and cardiovascular diseases. ����ʊ��, ��85����{�z��w���i2021�N3��26�`28���A���l�j
- Koga J, Katsuki S, Matoba T, Tsutsui H. Notch Ligand Delta-like Ligand 1 Promotes Macrophage Activation and Arteriosclerosis. American Heart Association 2020 (November 13-17, 2020, USA, virtual)
- Koga J, Umezu R, Katsuki S, Matoba T, Tsutsui H. Dynamin-related protein 1 induces macrophage activation and intimal hyperplasia after mechanical injury in mouse femoral arteries. Vascular Biology 2020 (October 26-29, 2020, USA, virtual)
- �Éꏃ��Y�C�I��N�ƁC�@�V�މ��C�쑺����C�]������C����T�V. �~�g�R���h���A�_�C�i�~�N�X�ɂ��}�N���t�@�[�W�@�\����ƌ��Ǖa. �V���|�W�E��, CVMW2019. 2019�N12��14���C�_��
- Umezu R, Koga J, Tsutsui H, Egashira K. Deletion of cyclophilin d inhibits atherosclerotic plaque formation in apolipoprotein-e deficient mice. ESC Congress 2018. 2018.8.27. Munich, Germany.
- Fujiwara M, Matoba T, Koga J, Okahara A, Funamoto D, Nakano K, Tsutsui H, Egashira K. Nanoparticle-mediated delivery of toll-like receptor 4 antagonist to monocytes and ischemic myocardium enhances cardioprotection against ischemia-reperfusion injury in mice. ESC Congress 2018. 2018.8.26. Munich, Germany.
- Okahara A, Matoba T, Koga J, Fujiwara M, Funamoto D, Nakano K, Tsutsui H, Egashira K. Nanoparticle-mediated simultaneous targeting of mitochondria and inflammatory monocytes protects the brain from ischemia-reperfusion injury in mice. ESC Congress 2018. 2018.8.26. Munich, Germany.
- �Éꏃ��Y�C�~�×����C�I��N�ƁC�]������. �~�g�R���h���A�Ɖ��ǁE�����d��. ��50�����{�����d���w���ACutting-Edge Symposium9�u�}�N���t�@�[�W�����̍őO���v 2018�N7��13��. ���.
- �Éꏃ��Y�C�~�×����C�I��N�ƁC����T�V, �]������. Macrophage dynamin-related protein 1, a mitochondrial fission protein, accelerates inflammation and neointimal thickening after vascular injury. ��82����{�z��w��w�p�W��. �V���|�W�E��15, �u���Ǐ�Q�Ɖ��ǁE�Ɖu�v 2018�N3��25��.